Vous êtes ici
Prédiction de la rechute métastatique dans les GIST : Projet CINSARC (Complexity INdex in SARComas) - Dr Frédéric Chibon
Le Dr Frédéric Chibon, biologiste moléculaire à l'Institut Bergonié (Bordeaux) et coordonnateur du projet CINSARC, nous parle de la découverte d'une signature moléculaire qui pourrait bien, dans l'avenir, supplanter les classifications actuelles pour devenir l'outil de référence pour l'évaluation du risque métastatique dans les GIST...
 Les GIST sont à ce jour les seuls sarcomes à bénéficier d’une thérapie ciblée particulièrement efficace : le Glivec®.
Les GIST sont à ce jour les seuls sarcomes à bénéficier d’une thérapie ciblée particulièrement efficace : le Glivec®.
Cette molécule permet en effet de cibler un des évènements oncogènes majeurs des GIST : l’activation par mutation du récepteur c-Kit.On comprend donc que tout GIST porteur d’une telle mutation (80%) est susceptible de bénéficier de cette thérapie.
Dans la pratique, ce traitement n’est nécessaire que pour les GIST très agressifs, c'est-à-dire :
- soit en situation métastatique au diagnostic,
- soit avec un haut risque de développer une métastase.
Toute la question est donc maintenant de pouvoir estimer ce mauvais pronostic et ensuite d’adapter la thérapie proposée aux patients.
Actuellement, le risque métastatique est évalué d’après la classification dite de « Miettinen » qui repose essentiellement sur trois facteurs :
1. la localisation de la tumeur,
2. sa taille
3. son index mitotique (c'est-à-dire une mesure indirecte de la vitesse à laquelle se divisent les cellules de la tumeur).
Selon cette classification, seuls les patients classés à « haut risque » (probabilité de développer une métastase= env 60%) seront traités par le Glivec® après exérèse chirurgicale de la tumeur tandis que les patients classés à « faible risque » (risque métastatique inférieur à 10%) ne seront traités que par la chirurgie.
Cependant, bien que cette classification présente l’avantage d’être très simple, peu coûteuse et de très bien fonctionner, elle comporte néanmoins deux inconvénients non négligeables :
1. Elle génère un groupe de pronostic intermédiaire dont la prise en charge n’est pas nécessairement la plus adaptée car le consensus médical actuellement suivi en France et en Europe est de traiter ces patients alors même que l’efficacité thérapeutique de l’imatinib au sein de cette population reste encore à démontrer.
2. Ainsi, 2/3 de ces patients sont traités alors qu’une meilleure évaluation de leur risque métastatique aurait pu éviter cette thérapie lourde, et onéreuse pour la société.
Au cours des deux années précédentes, nous avons mené en collaboration avec l’Institut Curie et l’ensemble du Groupe Sarcome Français une étude portant sur près de 200 sarcomes dits « à génétique complexe » (c'est-à-dire des tumeurs présentant de nombreuses anomalies chromosomiques à ce jour majoritairement non caractérisées) et de mauvais pronostic.
Par l’analyse de leurs profils :
- génomiques (ensemble des altérations chromosomiques présentes dans la tumeur)
- transcriptomiques (ensemble des gènes exprimés, c'est-à-dire jouant un rôle, par les cellules tumorales),
nous avons pu identifier un groupe de 67 gènes, impliqués dans le contrôle de la division cellulaire et l’intégrité des chromosomes, dont l’expression est étroitement corrélée :
1. d’une part, au nombre d’altérations portées par la tumeur
2. d’autre part, au risque métastatique.
Nous avons montré que l’ensemble de ces 67 gènes, qui constitue une « signature moléculaire », permet de classer ces sarcomes en deux groupes pronostiques à 5ans clairement différents :
- Groupe dit « à faible risque » : 20% de risque métastatique à 5 ans
- Groupe dit « à risque élevé » : 60% de risque métastatique à 5 ans.
Afin de valider cette « signature » dans l’ensemble des sarcomes et bien entendu dans les GIST, l’équipe sarcomes de l’institut Bergonié et moi-même avons donc décidé de développer le projet « CINSARC » (C omplexity IN dex in SARC omas), en grande partie financé par l’ INCa , la DHOS (Appel d’offre conjoint) et le réseau Européen CONTICANET , pour une durée de 3 ans.
Lorsque nous avions appliqué cette signature à une première série de 32 GIST (publiée par une autre équipe mais dont les données étaient librement accessibles), nous avions observé qu’elle permettait une classification des patients en deux groupes de pronostic très distincts puisque :
- aucun patient ainsi classé « à faible risque » n’a développé de métastase
- alors que 80% des patients classés « à risque élevé » présentent actuellement une évolution très péjorative.
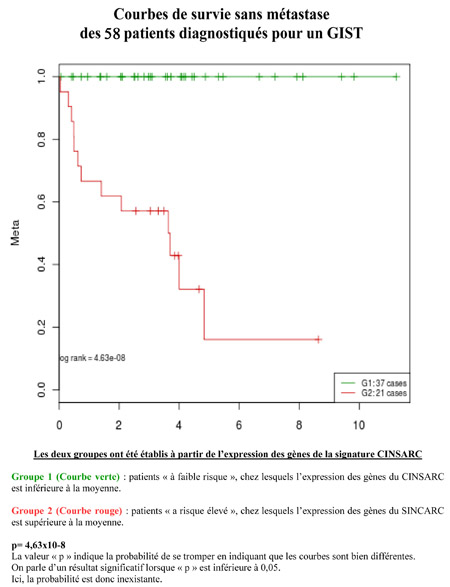
Afin de pousser plus loin notre évaluation, nous avons décidé à travers le projet CINSARC, d’engager une étude européenne par le biais du réseau CONTICANET .
Ce partenariat nous a ainsi permis d’analyser une série de 62 patients supplémentaires, grâce aux tumeurs fournies par le Dr Maria Debiec Richter (Louvain, Belgique) et d’asseoir la pertinence de la signature moléculaire dans la prédiction du risque de rechute métastatique (voir le tableau ci-contre).
Partant de ces premiers résultats encourageants, nous souhaitons désormais élargir cette série en ouvrant de nouvelles collaborations, notamment avec le Pr. Jean-François Emile (Hôpital Ambroise Paré, Boulogne-Billancourt) et d’autres partenaires du GSF-GETO et de CONTICANET afin d’accéder à un plus grand nombre de GIST.
Par la suite, nous souhaitons établir les profils génomiques de ces GIST afin de pouvoir appliquer, à terme, cette signature moléculaire en routine diagnostique.
Nous pensons que cette nouvelle démarche permettrait ainsi de mieux cibler les patients à traiter, c'est-à-dire :
- de ne pas traiter inutilement les patients qui n’ont aucun risque de faire une rechute locale ou à distance ;
- et au contraire de traiter de manière appropriée les patients pour lesquels ce risque est avéré.
Selon nos estimations actuelles, l’application de cette signature moléculaire éviterait à environ 20% des patients (actuellement traités d’après la classification de Miettinen) de recevoir un traitement lourd et particulièrement coûteux qui, aux vues de leur situation médicale, ne présenterait finalement aucun intérêt, ni bénéfice thérapeutique.




